
Доклад специалистов Клиники МАМА на 15 всемирном конгрессе в области гинекологической эндокринологии (15 WORLD CONGRESS OF GINECOLOGICAL ENDOCRINOLOGY). 07-10 марта 2012, (Флоренция, Италия)
ВВЕДЕНИЕ
Цитоплазматическая фрагментация - явление, часто встречающееся у доимплантационных эмбрионов человека invitro, снижающее их жизнеспособность и вероятность наступления беременности. Одной из возможных причин фрагментации является программируемая клеточная гибель. Повышение уровня экспрессии генов апоптоза в ходе оогенеза зависит от внешних факторов, влияющих на процесс созревания ооцита (гормональное и гомеостатическое воздействие, интоксикации). В программах лечения бесплодия методам ЭКО созревание большего количества ооцитов индуцируют повышенными дозами гонадотропных гормонов, многие пациентки имеют нарушения в эндокринной системе, страдают эндометриозом и синдромом поликистозных яичников. Эти факторы могут являться причиной сверхэкспрессии некоторых генов апоптоза в ходе оогенеза.
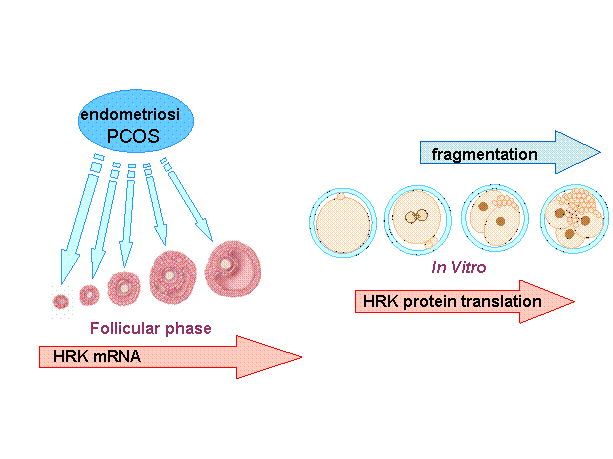
Анализ паттернов экспрессии генов клеточной гибели в период доимплантационного развития человека показал, что в ооцитах и ранних эмбрионах, наряду с мРНК генов, регулирующих процесс дробления, присутствуют мРНК некоторых генов, участвующих в активации и реализации программы клеточной гибели. Показано, что в эмбрионах, фрагментация которых начиналась еще со стадии зиготы, уровень экспрессии мРНК генов, подавляющих апоптоз, снижен, в то время как содержание мРНК основных генов программируемой гибели - повышено. Так, во фрагментирующихся эмбрионах человека было показано усиление синтеза запускающего апоптоз белка Harakiri (HRK).
Открытиями последних десятилетий в области генетики и молекулярной биологии показана возможность регуляции экспрессии белка экзогенными нуклеиновыми кислотами, что положило начало развитию нового направления молекулярной медицины. Преимущество подхода антисмыслового ингибирования на посттранскрипционном уровне заключается в том, что в результате воздействия терапевтического не затрагивается целостность генома, так как все биохимические процессы протекают вне ядра: в клетку вводится АсОДН, которая комплементарно связывается с мРНК в цитоплазме, образуя двуцепочечный комплекс, что препятствует синтезу белка.
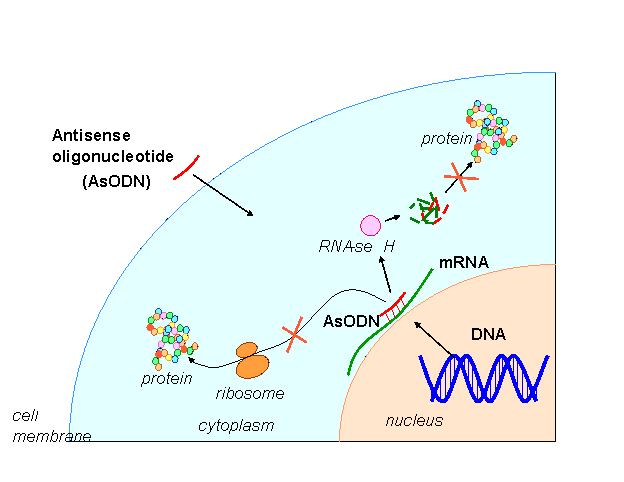
Мы исследовали возможность регуляции синтеза белка HRK в клетках доимплантационных эмбрионов человека и разработали новую модификацию среды для культивирования эмбрионов, содержащую новый компонент – АсОДН к мРНК HRK.
МЕТОДЫ
В исследование была включена 91 пациентка в возрасте от 19 до 44 лет, проходящих лечение бесплодия методом ЭКО. Причиной бесплодия были синдром поликистозных яичников, эндометриоз или сочетание перечисленных факторов. Индукцию суперовуляции проводили со 2-3 дня цикла преимущественно по короткому протоколу с использованием препаратов гонадотропинов, рекомбинантных ФСГ, препаратами ХГЧ, менопаузальными гонадотропинами.
Модификация среды. Синтез олигонуклеотидов был осуществлен на автоматическом синтезаторе амидофосфитным методом. АсОДН к мРНК гена HRK человека были добавлены в концентрации 0,13 nmol/ml в среду для культивирования гамет, зигот и эмбрионов человека (BlastAssist System, MediCult, Denmark).
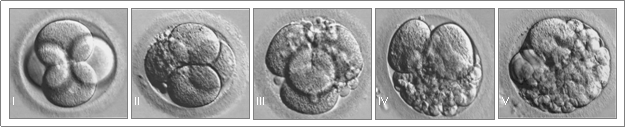
Культивирование и оценка качества эмбрионов. Ооциты и эмбрионы культивировали в среде с добавлением АсОДН (экспериментальная группа) с момента получения ооцитов и в течение 48 часов после оплодотворения invitro, дальнейшее культивирование эмбрионов до внутриматочной трансплантации осуществляли в среде без АсОДН. Ооциты и эмбрионы контрольных групп культивировали с момента получения ооцитов либо в среде с добавлением смысловой последовательности (неспецифический контроль), либо в среде без добавления нуклеотидов (интактный контроль). При оценке качества эмбрионы разделяли на пять групп: эмбрионы без фрагментации бластомеров (I), степень фрагментации < 10% объема эмбриона (II), 10-25% объема эмбриона фрагментировано (III), 25-50% объема эмбриона фрагментировано (IV), степень фрагментации >50% (V).
РЕЗУЛЬТАТЫ
Сравнение клинико эмбриологических показателей в группах.При статистическом сравнении групп пациенток с помощью t-критерия Стьюдента и точного двустороннего критерия Фишера не выявлено достоверных возрастных различий между экспериментальной и контрольными группами. Также показано, что между группами нет достоверных различий по причине бесплодия, количеству ооцитов, полученных в ходе программы ЭКО, и индексу нормального оплодотворения. Полученные при сравнении групп данные позволяют предположить, что приведенные далее результаты отражают терапевтический эффект от воздействия АсОДН на развивающиеся эмбрионы человека in vitro.
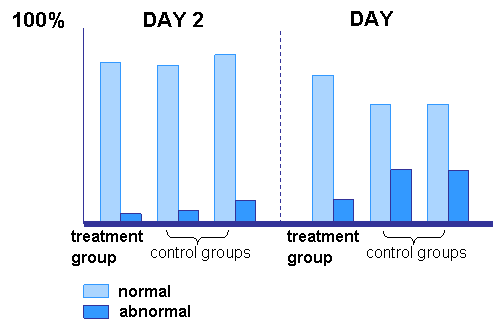
Сравнение качества эмбрионов между группами на 2 и 3 сутки развития.В ходе статистического анализа эмбрионы без фрагментации или с фрагментацией <25% были охарактеризованы, как «нормальные эмбрионы», а эмбрионы с аномальным развитием или со степенью фрагментации > 25% - как «аномальные эмбрионы». Показано, что на третьи сутки развития в экспериментальной группе достоверно больше эмбрионов без фрагментации (86,8%), чем в группе интактного контроля (69,3%) и группе неспецифического контроля (69,5%). Контрольные группы по состоянию эмбрионов на третьи сутки развития не отличаются.
Наступление беременности.В экспериментальной группе беременность наступила у 18 из 34 пациенток, что составило 52,94%, в группе интактного контроля – у 11 из 36, что составило 30,56%, а в группе неспецифического контроля – 4 из 21 (19,05%).
Доклад специалистов Клиники МАМА на 15 всемирном конгрессе в области гинекологической эндокринологии

Главный вход на 15 всемирный конгресс в области гинекологической эндокринологии
Стендовый доклад специалистов Клиники МАМА на 15 всемирном конгрессе в области гинекологической эндокринологии